3月の論文紹介まとめ
医局SNSでは適宜論文紹介を行っております。紹介する論文は、新しい論文で医局員がオモシロイと思ったものです。
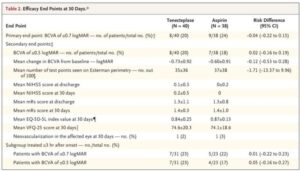
1.A Randomized Trial of Tenecteplase in Acute Central Retinal Artery Occlusion.
※詳細は以下のリンク先をクリックしてご覧ください。
https://pubmed.ncbi.nlm.nih.gov/41604638/
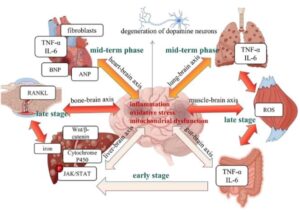
2.Beyond the Brain: Exploring the multi-organ axes in Parkinson’s disease pathogenesis.
※詳細は以下のリンク先をクリックしてご覧ください。
https://pmc.ncbi.nlm.nih.gov/articles/PMC12869220/
3.Comparative Effectiveness of Disease-Modifying Treatments in Double Seronegative Neuromyelitis Optica Spectrum Disorder.
※詳細は以下のリンク先をクリックしてご覧ください。
4.Effectiveness of Levetiracetam vs Valproic Acid for Poststroke Seizure: A Population-Based Study Using a Target Trial Emulation Framework.
※詳細は以下のリンク先をクリックしてご覧ください。
https://pubmed.ncbi.nlm.nih.gov/41183250/
一覧はこちら